Aún más, estos anticuerpos pueden ser hallados hasta en un 30% en adultos sanos, cuando el substrato utilizado es HEp-2. Debido a la alta sensibilidad de este sustrato, aún pequeñas cantidades de ANA presentes en pacientes y controles, pueden generar muestras positivas no relacionadas a patología. En la práctica diaria es frecuente hallar un ANA con patrón nuclear fino denso en mujeres jóvenes, pero éstas no siempre tienen criterios diagnósticos para enfermedad reumática, quienes luego de observaciones reiteradas a largo plazo, permanecen asintomáticas.
¿Que son los anti-DFS70?
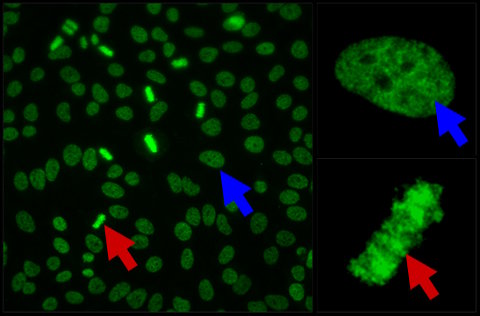
El nombre está dado por el patrón o imagen característica por IFI, que es reconocido como moteado denso fino, distribuido uniformemente por todo el núcleo en interfase y en la cromatina metafásica. Este patrón nuclear de ANA por IFI está asociado a anticuerpos dirigidos al antígeno DSF70. Luego del reconocimiento de esta proteína de 70-kDa por Inmunoblotting (IB), el antígeno se denominó Dense Fine Speckles 70 o DFS70. El mismo antígeno es conocido como “Lens Epithelium Derived Growth factor” (LEDGFp75) o “DNA binding transcription coactivator p75”, el que presenta numerosas funciones fisiológicas, dentro de las que constan: servir como cofactor de replicación del virus VIH a través de su interacción con la integrasa viral, también promover la supervivencia de las células y mejorar la resistencia al estrés celular. Es posible que estos anticuerpos sean gatillados por factores ambientales. Recientes observaciones han involucrado al virus HPV como activador de los mismos.
¿Cuál sería la utilidad clínica de los anti-DFS70?
En los últimos años distintos investigadores, han propuesto a los anticuerpos anti-DFS70 como marcadores biológicos útiles, para excluir a los pacientes con SARD. Esta sugerencia principalmente se ha basado en la observación de que estos anticuerpos son más frecuentes en individuos sanos que en los pacientes con SARD y que los individuos anti-DFS70 positivos no desarrollaron SARD, después de un seguimiento clínico por cuatro años.
¿Los anti-DFS70 serían anticuerpos protectores?
Algunos investigadores han sugerido la hipótesis que serían autoanticuerpos protectores. La posibilidad de incrementar la especificidad del ANA positivo, mediante una prueba de laboratorio, resulta muy tentadora; de este modo se evitaría tanto la incertidumbre en los pacientes como en los médicos y el incremento de los gastos en salud.
¿Puede detectarse Anti-DFS70 a través de patrones de IFI?
Los Anti-DFS70/LEDGFp75 son detectados mediante substratos HEp-2 por IFI y se observan como un patrón moteado fino denso. La prevalencia de su imagen de fluorescencia, muestra una significativa variabilidad en cuanto a los resultados en células HEp-2, de diferentes marcas. Estas variaciones pueden ser atribuidas a la fijación de los sustratos celulares y las condiciones de cultivo, entre otros.
¿Cuándo se debe usar un test confirmatorio de DFS70?
Actualmente, crece el consenso que los tests ANA no deben ser utilizados como método único, para la detección de los anti DFS70/LEDGFp75. Otros tests son necesarios para lograr una adecuada confirmación. En la actualidad se utilizan varios métodos para su detección: IFI, Inmunoblotting (IB), ELISA, Quimioluminiscencia como test confirmatorio.
¿Cuál es la presentación clínica de los anti-DFS70 en los pacientes?
Ocurren en pacientes, con una variedad de condiciones inflamatorias crónicas: cistitis intersticial, dermatitis atópica, alopecía areata, enfermedad de Behcet, enfermedades oculares y pacientes con cáncer. Además es hallado en el 10% de individuos sanos. En un estudio, se han detectado anticuerpos anti-DFS70 en el 11% de 597 trabajadores de los hospitales japoneses, pero en sólo alrededor del 2% de los pacientes con SARD. La causa de la baja prevalencia observada en SARD no es clara, sin embargo, incluyen factores demográficos, étnicos, influencia terapéutica y sin duda, el método utilizado para la detección de auto anticuerpos.
Dellavance y col, han evaluado más de 10000 muestras ANA positivos por IFI e IB, informando que los anticuerpos anti-DFS70 eran comunes entre individuos ANA-positivos, sin evidencia de SARD. Los pacientes con patología autoinmune que presentaban estos anticuerpos, más de la mitad tenían evidencia de tiroiditis autoinmune. La mayor prevalencia de anticuerpos anti-DFS70, ha sido reportada en pacientes con síndrome de Vogt-Harada (66,7%) y la dermatitis atópica (30%), seguido de los individuos aparentemente sanos (~ 10%), mientras que la prevalencia en la SARD es significativamente inferior (~ 2% -3%) y a diferencia de los resultados de ANA que aumentan su positividad con la edad en individuos sanos, los anti-DSF70 decrecen en esta circunstancia.
Se informó recientemente que ninguno de los individuos sanos, con anti-DFS70 positivos como hallazgo aislado desarrolló un SARD, luego de cuatro años de seguimiento promedio. Por lo tanto, se sugirió que la presencia de anticuerpos anti-DFS70 aislados, podría ser interpretada como una fuerte evidencia en contra de un diagnóstico de una SARD o sea serian marcadores de exclusión de SARD.
¿Cuál es la relación entre anti DFS70 y SARD?
En pacientes con SARD confirmada, se analizó la presencia simultánea de varios auto anticuerpos relacionados y de anti-DFS70. En 472 pacientes con SARD sistémica, los anticuerpos anti-DFS70 fueron encontrados en 21 pacientes (4,4%). De estos 18 de los 21 (86%) pacientes fueron positivos, asimismo, para otros auto anticuerpos relacionados con la SARD, tales como anti-DNA de doble cadena y anti-SS-A. Aunque los pacientes con síndrome Sjögren tenían la mayor frecuencia de anti-DFS70 (11%, 8/71), sólo uno de los ocho pacientes con anticuerpos anti-DFS70 no tenía anti-SS-A. Los anti-DFS70 se han hallado en 3% de pacientes con LES, asimismo asociados a otros auto anticuerpos marcadores con anti-DNA doble cadena, anti-SSA/ Ro o anti-Sm.
En un estudio de 116 pacientes con dermatomiositis (DM), sólo 7 fueron positivos para anti-DSF70 (6,4%) confirmados por inmunoblotting (IB) y 5 de ellos eran acompañados por otro auto anticuerpo específico para DM. La hipótesis sería que el anti-DSF70 sirve como anticuerpo protector, respaldado por su mayor prevalencia en pacientes sanos que en pacientes con SARD.
En otro estudio también se observa que, más del 80% de los pacientes con SARD confirmada y presencia de anti-DFS70 presentan simultáneamente, otros auto anticuerpos marcadores de SARD. En base a estos reportes, se considera que los pacientes con SARD y anti DFS70 positivo como hallazgo aislado, deberían ser raros tanto en niños como en adultos. Aún más, ciertos autores plantean que si un paciente tiene anti-DFS70 como anticuerpo aislado, no tiene necesidad de interconsulta urgente con el especialista.
¿Cuán frecuente es observado el patrón DFS70 en la rutina del laboratorio de autoinmunidad?
Los Anti-DFS70 son responsables de más del 12 % de los resultados de Hep2 positivos. Asi la alta prevalencia de los mismos es un reflejo de la alta frecuencia de estos autoanticuerpos en la población general. En estudios publicados por Watanabe,los anti-DFS70 representan el 54% de los ANA positivos en los sujetos sanos con test de ANA positivo.
¿Cuál sería el algoritmo diagnóstico de los anti DFS70?
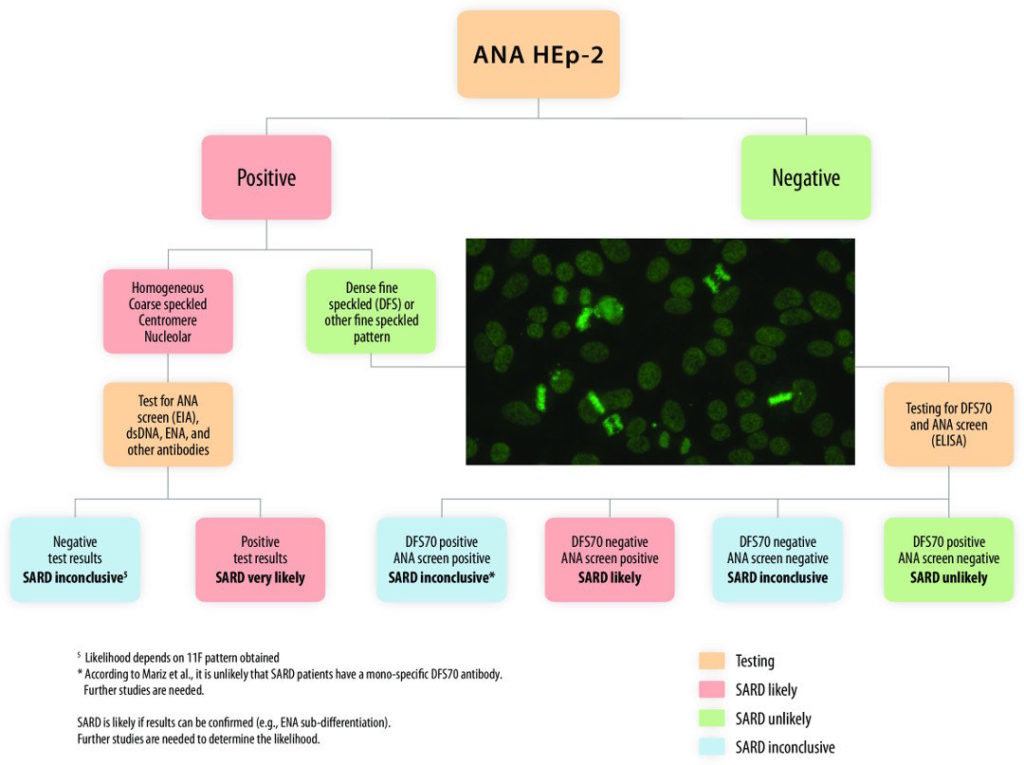
Muestras con patrones moteados finos denso deben ser testeados para anti-DFS70 por un test confirmatorio y un ANA screen conteniendo varios autoantigenos.
Los pacientes con ANA screen negativos y DSF-70 positivo presentan baja probabilidad de tener SARD. Los pacientes con ANA positivo ya sea en combinación con un DSF-70 positivo o negativo resulta de un incrementada probabilidad de tener SARD.
Dado que una prueba de ANA positiva es un componente importante en la clasificación y diagnóstico de pacientes con posible SARD, un ANA realizado en sustrato Hep – 2 pedido fuera del entorno clínico apropiado puede dar ANA positivo en un individuo sano, causando la preocupación y la ansiedad en los pacientes y los médicos. Por lo tanto, las muestras con un patrón de tinción aparente de DFS identificado por IFI, se debe realizar un test confirmatorio de anticuerpos anti- DFS70 por un ensayo de confirmatorio. Los médicos no deben sobrestimar los resultados positivos de ANA en pacientes con anticuerpos anti – DFS70 aislados y se deben centrar en los síntomas clínicos.
Resumiendo:
El reconocimiento del patrón DFS en los test de ANA, es importante para detectar la presencia de anti-DFS70. Un resultado de ANA positivo por IFI puede ser causado por diferentes autoanticuerpos incluyendo anti DFS70 que no está asociado con SARD. Un resultado positivo causado por estos autoanticuerpos contribuye a la ansiedad del paciente y del médico, agregando costos al sistema de salud. EL anti DFS70 aislado no se asocia con ninguna SARD. Los Anti-DFS70 son responsables de más de 12 % de los resultados ANA positivos. La medición de los anti-DFS70 elimina la necesidad de test reflejos y de test de seguimiento.
Como conclusión
Medir anti-DFS70 puede servir para excluir SARD. La presencia solitaria de anti DFS70, podría ser utilizado como biomarcador para excluir el diagnóstico de SARD, incluyendo estos anticuerpos en el chequeo de personas ANA positivo, se podría excluir la SARD y disminuir los gastos en salud.
Bibliografía:
-
Importance of the dense fine speckled pattern on HEp-2 cells and anti-DFS70 antibodies for the diagnosis of systemic autoimmune diseases Michael Mahler a, John G. Hanly b, Marvin J. Fritzler Autoimmunity Reviews 11 (2012) 642–645
-
Application of anti-DFS70 antibody and specific autoantibody test algorithms to patients with the dense fine speckled pattern on HEp-2 cells H Lee, Y Kim, K Han & E-J Oh Scand J Rheumatol 2015;00:1–7
Autor: Dra. Patricia Gentili – Jefa del Área Inmunología – Fares Taie Instituto de Análisis. Especialista en Inmunología Clínica
Fuente: Fares Taie Biotecnología